المول والمقادير المولية
-
1. la mole , l'unité de la quantité de la matière :
-
1.1. Définition de la mole :
Une mole est la quantité de matière dans un groupe contenant un nombre de constituants élémentaires égal au nombre d'atomes présents dans 12g de le carbone
 .
. -
1.2. Constante d'avogadro :
La constante d'avogadro est: NA=6,02.1023mol-1.
-
1.3. La relation entre la quantité de matière et la constante d'Avocado :
la quantité de matière dans un échantillon de substance X qui contient N des constituants elementaires est :
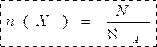
-
-
2. Masse molaire atomique et masse molaire moléculaire :
-
1.2. Masse molaire atomique :
Nous appelons la masse molaire atomique d'un élément chimique la masse d'une mole des atomes de cet élément. .
-
2.2. masse molaire moléculaire :
On appelle masse molaire d'un corps pur, la masse d'une mole des molécules de ce corps.
Elle est égale à la somme des masses molaires atomiques des atomes qui composent la molécule
-
3.2. La relation entre la quantité d'une substance et la masse molaire :
ON Détermine la quantité de matière n(X)، pour une substance X de masse m(X) avec la relation:
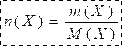
-
-
3. Le volume molaire d'un gaz :
-
1.3. définition :
On appelle volume molaire VM le volume occupé par une mole de différents gaz dans les mêmes conditions de température et de pression
Le rapport entre la quantité de gaz et son volume V et son volume molaire VM :
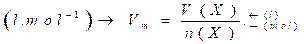
-
2.3. Loi d'avogadro-Ampre :
La même quantité de matière de différents gaz dans les mêmes conditions de température et de pression occupe le même volume
Autrement dit, à température et pression constantes, différents gaz de volumes égaux contiennent un nombre égal de molécules.
-
3.3. Densité du gaz par rapport à l'air :
C'est le rapport de la masse d'un volume de gaz donné à la masse du même volume d'air, dans les mêmes conditions de température et de pression

où m :est la masse du volume de gaz. et m’ : la masse d'un même volume d'air .
Dans les conditions normales :

-